

Chapitre 2 - Justesse
Valeur vraie et Valeur conventionnelle
Dans le domaine de la biologie médicale, il n’existe pas toujours de matériau de référence certifié, comme c’est le cas pour le kilo ou le mètre par exemple. De plus, les procédures de mesure de référence ne sont pas utilisées en routine. Elles sont trop complexes, souvent chères et trop lentes. La notion de « valeur vraie » est donc assez floue. Il n’y a pas de consensus pour la définir clairement.
Selon le VIM, dans l'approche «erreur» de description des mesurages, la valeur vraie est considérée comme unique et, en pratique, impossible à connaître. L’approche «incertitude» consiste à reconnaître que, par suite de la quantité intrinsèquement incomplète de détails dans la définition d'une grandeur, il n'y a pas une seule valeur vraie mais plutôt un ensemble de valeurs vraies compatibles avec la définition. Toutefois, cet ensemble de valeurs est, en principe et en pratique, impossible à connaître.
La valeur conventionnelle, elle, est une valeur attribuée à une grandeur par un accord pour un usage donné.
Calcul du biais
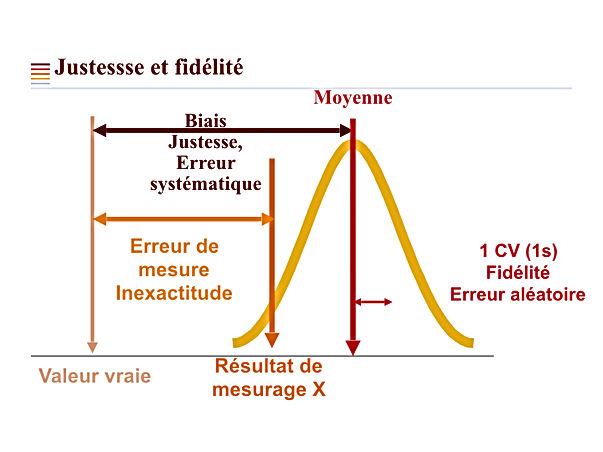
Le biais est la différence entre une moyenne de mesurages répétés et une valeur vraie. Il peut être exprimé en valeur relative ou absolue. Le biais est soit négatif si la moyenne des mesures est inférieure à la valeur vraie ou positif si la moyenne est supérieure à la valeur vraie.
Biais absolu = moyenne - valeur vraie, exprimé dans les unités de la mesure
Biais relatif = (moyenne - valeur vraie)/ valeur vraie
Par exemple :
-
Valeur vraie = 100 mmol/l
-
Valeur moyenne = 90 mmol/l
-
Biais absolu = 90 - 100 = –10 mmol/l
-
Biais relatif = (90 -100)/100 = -0,1 ou -10%

Aujourd’hui, c’est l’approche métrologie qui prévaut. Dans cette approche, la « valeur vraie » de l’étalon n’est pas connue, mais ce qui est certifié c’est que la valeur se situe dans un certain intervalle pour une probabilité donnée.
Le fabriquant d’une méthode doit dorénavant déterminer l’incertitude de sa méthode par rapport à l’étalon reconnu. Ainsi pour le glucose, l’étalon utilisé est le NIST SRM 965, la méthode de référence est ID-LC/MS (isotope dilution gas chromatography/mass spectrometry). L’incertitude de la méthode (pour k=2) est ±0.149 mmol/L pour l’étalon de 2.683 mmol/L et ±0.666 mmol/L pour l’étalon de 12.008 mmol/L.
Concept de traçabilité métrologique
L'objectif premier de la traçabilité métrologique est de garantir aux laboratoire de biologie médicale qu'ils produisent des résultats d'analyses qui soient à la fois comparables et transférables.
Sans traçabilité jusqu'à une procédure de mesure de référence ou un étalon, les cliniciens peuvent recevoir pour le même patient des résultats de laboratoires différents avec peu ou pas d’information sur la comparabilité des résultats.
Dans la société d'aujourd'hui, la mobilité des dossiers médicaux augmente du fait que les patients déménagent ou changent de laboratoire d'analyses. Lors d'un suivi médical, des décisions étant prises par rapport aux résultats obtenus auparavant pour le même patient, l'interprétation et le traitement corrects dépendent de la concordance des résultats entre différents laboratoires et entre différentes procédures de mesure.
La solution est l'harmonisation des analyses par rapport à une procédure de mesure de référence ou à un étalon. Dans l'exemple ci-dessous, le résultat A et le résultat B sont comparables parce que tous deux peuvent être rattachés à une procédure de mesure de référence ou un étalon commun.
Il consiste à s’assurer qu’un résultat de mesure est relié à une référence par l’intermédiaire d'une chaîne ininterrompue et documentée d’étalonnages. La norme ISO 17511 a décrit de concept.




Calcul du biais sur la base du contrôle qualité
En pratique, en Suisse, pour les comparaisons interlaboratoires, la « valeur vraie », considérée comme une valeur consensuelle, est définie comme la moyenne du groupe des pairs. Les pairs étant les laboratoires qui utilisent les mêmes méthodes de mesure. L’organisme chargés des comparaisons interlaboratoires envoie un échantillon identique à plusieurs laboratoires. Le but est d’imiter un patient qui se présenterait au même moment à tous les laboratoires participant aux comparaisons interlaboratoires. Chaque laboratoire effectue les examens (par exemple le glucose) comme il le ferait pour un patient. Les résultats sont ensuite envoyés à l’organisme de comparaisons interlaboratoires. Ce dernier récolte les résultats et calcule la moyenne obtenue par touts les laboratoires (avec les précautions statistiques nécessaires), toutes méthodes confondues, puis la moyenne obtenue pour chacune des méthodes d’analyses, qui peuvent parfois être regroupées. Le résultat transmis par chaque laboratoire est ensuite comparé à la moyenne des pairs.
Il est très rare de pouvoir utiliser la moyenne de tous les laboratoires comme valeur vraie. La raison principale étant que l’échantillon de contrôle n’est pas parfaitement similaire au sang humain.




Il contient des stabilisateurs et autres substances qui provoquent des « effets de matrice ». Ainsi, deux méthode de mesure différentes vont mesurer une concentration de glucose différente dans un échantillon de contrôle (un matériau de référence), alors que sur un échantillon de patient les résultats auraient pu être beaucoup plus semblables. Il s’agit d’un défaut de commutabilité. L’autre raison est que certaines méthodes d’analyses donnent des résultats différents sur les échantillons de patients également, mais qu’une procédure de mesure ne peut pas être considérée comme meilleure que l’autre. En Allemagne, l’approche est différente et lorsqu’il existe une procédure de mesure de référence, c’est le cas pour le glucose, un échantillon de contrôle est envoyé à plusieurs laboratoires de référence qui vont déterminer la concentration du glucose avec la procédure de mesure de référence et ainsi définir une valeur vraie (et son incertitude) avec laquelle tous les laboratoires et toutes les méthodes d’analyses seront ensuite évalués.
Attention, la différence obtenue entre une seule mesure (ce qui est recommandé lors des comparaisons interlaboratoires) et une valeur vraie est l’inexactitude, à ne pas confondre avec la notion de justesse, mesurée par le biais, qui est une comparaison de la moyenne de plusieurs valeurs à une valeur vraie. Certains organismes de contrôle externe envoient donc plusieurs fois le même échantillon en cours d’année, par exemple 3 ou 4 fois, afin de pouvoir établir une moyenne et établir ainsi le biais. Il existe aussi une méthode de calcul qui permet d’estimer les biais sur la base de plusieurs enquêtes avec des échantillons de différentes concentrations.
Pour établir le biais, plusieurs fabricants de contrôle interne proposent d’envoyer tous les résultats obtenus lors de l’exécution du contrôle interne dans une base de données mondiale. Cela permet de des comparaisons entre groupes de pairs, soit tous les résultats provenant d’une même méthode sur un même instrument (par exemple le glucose par méthode hexokinase sur Architect). Il est possible de comparer les résultats entre les mêmes méthodes de mesure (par exemple méthode glucose Hexokinase sur Cobas, Architect ou RxL).
Par analogie aux comparaisons interlaboratoires, il est recommandé de considérer que la valeur vraie (ou valeur cible) d’un contrôle interne est la moyenne d’un groupe de pairs. La moyenne toutes méthodes confondues peut difficilement être prise en compte en raison de l’effet de matrice qui peut générer de grandes différences entre les méthodes, comme nous l’avons vu précédemment.
Certains laboratoires considèrent que la valeur annoncée par le fabriquant de contrôle est la valeur vraie mais cela n’est correct que si le contrôle est certifié, ce qui est rarement le cas.
A défaut de base de données disponible, il est acceptable d’utiliser la valeur donnée par le fabriquant à titre informatif. La règle est que la moyenne obtenue au laboratoire doit se situer dans l’intervalle annoncé.
Biais établi sur la base d’une méthode de référence
Il s’agit de sélectionner des échantillons de patients sur toute la gamme de mesure, en particulier sur les seuils décisionnels. Idéalement les échantillons doivent être représentatifs de la population rencontrée au laboratoire. Pour un hôpital, par exemple, il est important d’inclure des échantillons provenant des soins intensifs, de la dialyse, des urgences, etc. La quantité d’échantillons à tester dépend des différences entre les méthodes. Plus les différences sont importantes, plus le nombre échantillon doit être augmenté. Il faut aussi tenir compte de la stabilité des échantillons. L’idéal étant de travailler sur du matériel frais, qui n’a pas été congelé et de réaliser les analyses avec les 2 méthodes dans le même laps de temps. Les résultats sont ensuite comparés et représentés dans un graphique. Calculer et représenter la droite de régression linéaire et calculer le facteur de corrélation. « a » est la pente de la droite correspondant à l’erreur systématique proportionnelle et b est l’ordonnée à l’origine correspondant à l’erreur systématique constante. Il faut noter que la régression linéaire et le graphique des différences sont réservés aux comparaisons avec une méthode de référence. Dans tous les autres cas (comparaison entre ancienne et nouvelle méthode par exemple) il est recommandé de faire une régression selon Passing-Bablok (ou selon Deming, régression des moindres rectangles selon Tessier, etc.) et une diagramme de Bland et Altman. Si la méthode évaluée est identique à la méthode de référence la pente vaut 1 et l’ordonnée à l’origine 0. Les différences valent toutes 0.
Exemple de biais déterminé par une méthode de référence :

Le biais est nul car la pente de la droite de régression vaux y=x.
En dehors du cas où y=x, il est possible de calculer le biais sur les différents seuils décisionnels en appliquant la formule de la droite de régression obtenue. Dans le cas où la droite vaux y=1.1x+0 il faut multiplier la valeur obtenue par la méthode de référence, soit 6 mmol/l par 1.1 et ajouter 0. Le résultat obtenu est la valeur y, qui correspond à la valeur théorique (moyenne) obtenue avec la méthode évaluée. Dans l’exemple ci-dessous « y » vaut 6.6 mmol/l. Une fois ces deux valeurs obtenues le calcul du biais est classique.
 |  |  |
|---|---|---|
 |  |  |
 |  |  |
 |
Biais établi sur la base de deux méthodes, par exemple actuelle et nouvelle méthode
Dans ce cas il n’est pas correct de considérer une méthode comme plus juste que l’autre.
En conséquence le graphique des différences sera remplacé par le diagramme de Bland et Altman, qui utilise la moyenne des résultats obtenu par les 2 méthodes comme valeur la plus juste. La régression linéaire sera remplacée par une comparaison selon Passing-Bablok, qui donne autant de poids aux deux méthodes. Le biais se calcule comme précédemment à partir de la droite obtenue selon la méthode de régression choisie.